GEOCHEMICKÉ MODELOVÁNÍ PROCESŮ PROBÍHAJÍCÍCH NA PROPUSTNÝCH REAKTIVNÍCH STĚNÁCH PRO SANACI ROZPUŠTĚNÝCH CHLOROVANÝCH UHLOVODÍKŮ
Petr Kozubek
AQUATEST a.s., Geologická 4, 152 00 Praha 5,
e-mail: kozubek@aquatest.cz
Úvod
Chlorované uhlovodíky patří k nejběžnějším polutantům horninového prostředí. K sanaci podzemních vod kontaminovaných chlorovanými uhlovodíky může být použito klasické sanační čerpání, avšak dlouholeté zkušenosti z průběhu sanace těchto lokalit poukazují na nedostatky této metody. Z tohoto důvodu jsou stále více využívány nové sanační technologie. Jednou z nových metod pro sanaci chlorovaných uhlovodíků rozpuštěných v podzemní vodě jsou propustné reaktivní stěny.
Nejjednodušší formou je propustná stěna vyplněná reaktivním materiálem, která je instalována napříč směru proudění rozpuštěných chlorovaných uhlovodíků. Prouděním podzemní vody propustnou stěnou dochází ke kontaktu chlorovaných uhlovodíků s reaktivní výplní, čímž jsou chlorované uhlovodíky rozkládány na netoxické nechlorované uhlovodíky a anorganické chloridy. Hlavní výhodou tohoto systému je, že není potřeba žádného čerpání nebo čištění odčerpaných vod. Protože tento systém nevyžaduje žádné nadzemní stavby, dotčené území může být využito k různým aktivitám, zatímco jsou podzemní vody sanovány. Dosavadní poznatky ukazují, že reaktivní výplň je spotřebovávána velmi pomalu, takže propustná reaktivní stěna může plnit svou funkci několik let až desítek let. Z toho vyplývá nenáročnost systému z pohledu provozních nákladů, které jsou tvořeny prakticky pouze náklady na monitoring.
Mechanismus odbourávání chlorovaných látek na propustných reakčních stěnách
Nejpoužívanějším reakčním médiem jsou nula mocné kovy, zvláště pak granulované železo. Korozí nula mocného kovu v reakční bráně dochází ke zvýšené elektronové aktivitě, která rozkládá chlorované uhlovodíky na netoxické produkty. Nejlépe je popsán proces rozkladu při použití granulovaného železa. Ostatní kovy mohou vyvolávat obdobné reakce s jinou rychlostí. Přesný mechanismus degradace chlorovaných látek železem nebo jinými kovy není úplně poznán. V každém případě se jedná o více cest rozkladu, přičemž některé z nich jsou dominantní. Např. Sweeny (1981) popsal reakci následovně:
Fe + H2O + RCl ® RH + Fe2+ + OH- + Cl-
Z rovnice je patrná degradace chlorovaného uhlovodíku (RCl) a oxidace železa za vzniku hydroxidových iontů a chloridů. Železo působí v reakci jako silné redukční činidlo, které reaguje s chlorovanými látkami, jež jsou z důvodu přítomnosti chlóru v oxidačním stavu. Uvolňované železo Fe2+ se může srážet ve formě minerálů železa jako jsou např. hematit, goethit apod. Produkce hydroxidových iontů OH- vede k nárůstu hodnoty pH, což může mít za následek vytváření dalších sraženin ve formě karbonátů (kalcit, siderit, dolomit) z důvodu poklesu alkality. Například vysrážení kalcitu probíhá podle následující rovnice:
Ca2+ + HCO3- + OH- ® CaCO3 + H2O
Prostředí v reaktivní části stěny je vysoce redukční a dochází tak k rychlé redukci přítomného kyslíku v přitékající vodě (za tvorby oxidů železa), dusičnanů, případně i síranů (redukce na sulfidy a vysrážení sulfidů železa pyritu nebo markazitu).
Tvorba sraženin může potenciálně významně snížit propustnost úvodní vrstvy reaktivní části stěny. Z tohoto důvodu je při rozhodování o použití reaktivních propustných stěn na konkrétní lokalitě významné ověření, k jakým změnám chemismu přitékajících vod může docházet. Jedním z prostředků pro toto posouzení je geochemické modelování.
Přístupy při geochemickém modelování
U geochemického modelování procesů probíhajících na propustných reaktivních stěnách lze rozlišit tři základní přístupy:
1. výpočet saturačních indexů (nezbytným vstupním údajem je chemismus vody v reakční části propustné stěny).
2. modelování reakce vstupní vody se železem (nezbytným vstupním údajem je chemismus podzemní vody posuzované lokality),
3. inverzní modelování (nezbytné jsou údaje chemismu jak vstupní vody tak vody v reakční části propustné stěny).
Jak vyplývá z výše uvedeného, je u dvou přístupů nezbytný údaj o chemismu vod v reakční části stěny. Ve fázi rozhodovacího procesu o použití technologie lze tento údaj získat na základě laboratorních zkoušek.
Kolonová zkouška
Pro plánovanou aplikaci technologie propustných reaktivních stěn pro sanaci rozpuštěných chlorovaných uhlovodíků byla provedena experimentální zkouška na zkušební aparatuře skládající se ze dvou dílů skleněné kolony. Přívod vody byl řešen hydrostatickým nátokem z nádoby s kontaminovanou vodou umístěné nad kolonou. Regulace průtoku byla prováděna pomocí tlačky.
V grafu č. 1 je ve formě výsledků laboratorních analýz vstupní a výstupní vody na obsah chlorovaných uhlovodíků znázorněna účinnost systémů při době zdržení 48, resp. 26 hodin.
V tabulce č. 1 jsou znázorněny rozdíly v chemismu vstupní a výstupní vody. Patrný je zejména výrazný pokles alkality, koncentrace vápníku, hořčíku, hodnoty Eh a nárůst koncentrace železa, chloridů a hodnoty pH.
Geochemické modelování
S údaji získanými z kolonové zkoušky bylo provedeno modelování pomocí geochemického modelu PHREEQC (Parkhurst, 1995) a to všemi třemi výše uvedenými přístupy.
Výpočet saturačních indexů
Saturační index SI udává vztah mezi reakčním kvocientem daného roztoku IAP a rovnovážnou konstantou K:
SI = log (IAP/K)
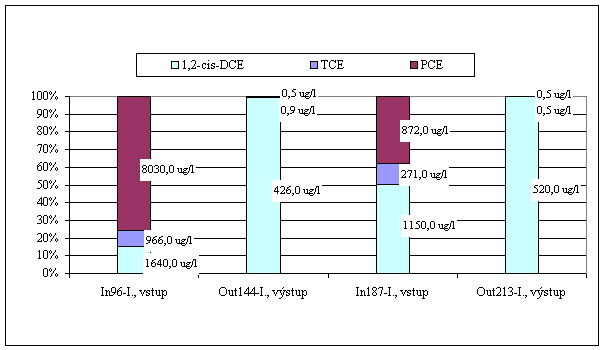
Graf č. 1: Porovnání vstupních a výstupních koncentrací ClU při kolonové zkoušce
Tabulka č. 1: Porovnání chemismu vstupní a výstupní vody při kolonové zkoušce (koncentrace v mg/l není-li uvedeno jinak)
|
Parametr |
vstup |
výstup |
|
pH |
7,1 |
9,8 |
|
Eh (mV) |
76 |
- 400 |
|
Dusičnany |
13,00 |
0,35 |
|
Alkalita (meq/l) |
7,66 |
0,45 |
|
Sírany |
121,00 |
139,00 |
|
Baryum |
0,21 |
0,03 |
|
Draslík |
1,70 |
3,20 |
|
Hliník |
0,05 |
0,12 |
|
Hořčík |
18,90 |
1,00 |
|
Sodík |
19,80 |
19,80 |
|
Vápník |
149,00 |
58,40 |
|
Mangan |
1,07 |
0,08 |
|
Železo |
0,01 |
3,3 |
|
Chloridy |
35,30 |
40,30 |
|
Kyslík |
1,5 |
- |
Při hodnotě SI = 0 je mezi roztokem a minerálem rovnováha (jako rovnovážný stav je obvykle uváděno rozmezí hodnot SI -0,2 až +0,2). Hodnoty SI < 0 znamenají nenasycení roztoku daným minerálem, tj. minerál se bude v daném roztoku rozpouštět, hodnoty SI > 0 indikují, že roztok je minerálem přesycen, tj. bude docházet k vysrážení minerálu.
Zadáním chemismu vody na výstupu z kolony (tabulka č. 1) bylo modelem odhadnuto, že výstupní voda je přesycena oxidy, resp. hydroxidy železa hematitem, goethitem, amorfním hydroxidem železitým a karbonáty aragonitem, kalcitem, dolomitem a sideritem (tabulka č. 2). U těchto minerálů lze tedy předpokládat, že bude docházet k jejich vysrážení. Nicméně odhad saturačních indexů neznamená, že k vysrážení daných minerálů bude skutečně docházet. Gavaskar et al. (1997) např. uvádí, že v systému aragonit/kalcit je aragonit nestabilní a lze jeho vysrážení opomenout.
Tabulka č. 2: Odhad saturačních indexů SI
|
Minerál |
SI |
log IAP |
log K |
Chemický vzorec |
|
Anhydrit |
-1.74 |
-6.08 |
-4.34 |
CaSO4 |
|
Aragonit |
0.78 |
-7.53 |
-8.31 |
CaCO3 |
|
Baryt |
0.08 |
-9.97 |
-10.05 |
BaSO4 |
|
Brucit |
-2.16 |
15.01 |
17.17 |
Mg(OH)2 |
|
Dolomit |
0.36 |
-16.61 |
-16.98 |
CaMg(CO3)2 |
|
Fe(OH)3(a) |
2.41 |
20.44 |
18.03 |
Fe(OH)3 |
|
Goethit |
8.13 |
20.44 |
12.31 |
FeOOH |
|
Hematit |
18.24 |
40.87 |
22.63 |
Fe2O3 |
|
Kalcit |
0.92 |
-7.53 |
-8.45 |
CaCO3 |
|
Manganit |
-6.40 |
18.94 |
25.34 |
MnOOH |
|
Melanterit |
-5.73 |
-8.00 |
-2.27 |
FeSO4:7H2O |
|
Rodochrozit |
0.16 |
-10.95 |
-11.11 |
MnCO3 |
|
Siderit |
1.41 |
-9.45 |
-10.86 |
FeCO3 |
|
Witherit |
-2.84 |
-11.42 |
-8.57 |
BaCO3 |
Modelování reakce vstupní vody se železem
Tento přístup je využíván v případech, kdy nejsou k dispozici údaje o chemismu vody v reakční části propustné stěny, resp. na výstupu z kolony. Vstupním údajem modelu je chemické složení vody posuzované lokality a simuluje se postupné přidávání nula mocného železa až k dosažení rovnováhy.
Do modelu bylo zadáno, že k rozpouštění železa dochází podle následující rovnice s konstantou rozpustnosti log K = 15,114 a entalpií DH = -21,3 kcal/mol (Ball et al. 1987).
Fe0 = Fe2+ + 2e-
V grafu č. 2 jsou znázorněny změny alkality a molární koncentrace síranů a hodnoty pH v závislosti na postupném přidávání nula mocného železa do roztoku. Z grafu je patrný nejprve prudký a poté pozvolný nárůst hodnoty pH a naopak pokles alkality a vyčerpání síranů.
V tabulce č. 3 je uvedeno porovnání vybraných parametrů chemického složení vody při dosažení rovnováhy s nula mocným železem (přidání cca 30 mmol/l Fe0), vody při dodání cca 3 mmol/l Fe0 vedoucí ke změně hodnoty pH na 9.8, což odpovídá hodnotě pH vody na výstupu z kolony a pozorovaných hodnot koncentrací ve vodě při kolonové zkoušce. Z porovnání je patrná výrazná disproporce mezi uvedenými údaji. Při kolonové zkoušce byl zaznamenán mnohem výraznější pokles alkality, relativně nízký nárůst koncentrace celkového železa a mírný nárůst v případě síranů. Tato disproporce znamená, že popis dějů geochemickým modelem pouze za simulace reakce vody s nula mocným železem je pravděpodobně vzhledem ke komplikovanosti dějů, které probíhají v reaktivní části propustných stěn, nedostačující a interpretace výsledků takového modelu může vést k chybným závěrům. Např. redukce síranů je biochemický proces, který je podmíněn přítomností baktérií rodu Desulfovibrio, což geochemický model nezohledňuje.
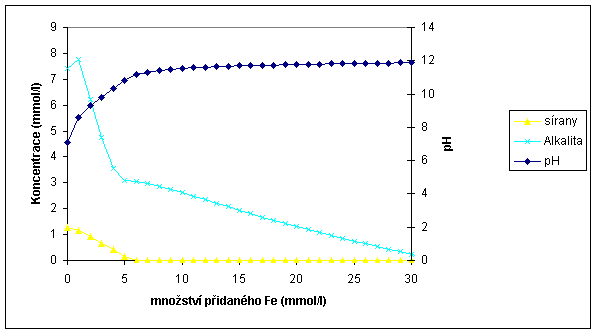
Graf č. 2: Vývoj změny alkality, koncentrace síranů a hodnoty pH v závislosti na přidávání Fe0 do roztoku
Tabulka č. 3: Porovnání pozorovaných hodnot na výstupu z kolony s odhady modelu
|
Parametr |
Výstup z kolony |
Rovnováha mezi roztokem a Fe0 |
Přidání 3 mmol Fe0 |
|
pH |
9,8 |
11,9 |
9,8 |
|
Alkalita (meq/l) |
0,45 |
0,24 |
4,75 |
|
Sírany (mmol/l) |
1,45 |
1,1.10-7 |
0,67 |
|
Celkové železo (mmol/l) |
0,059 |
30,0 |
3,0 |
Inverzní modelování
Inverzní modelování je odhad pravděpodobných reakcí vypočtených na základě porovnání změny chemismu vstupní a výstupní vody.
Při použití modulu inverzního modelování pro posuzovanou lokalitu však nebylo dosaženo konvergence a použití modelu tak bylo neúspěšné. Nedosažení konvergence je způsobeno pravděpodobně výrazným rozdílem hodnoty alkality a oxidačně redukčních podmínek mezi vstupní a výstupní vodou, na což je model PHREEQC nejvíce citlivý (Parkhurst 1995, Kozubek 1995).
Interpretace získaných údajů
Údaje získané z kolonové zkoušky a z výstupů modelu PHREEQC mohou být použity k odhadu snížení pórovitosti reakční části propustné stěny vlivem vysrážení minerálů.
V případě oxidu, resp. hydroxidů železa je postupováno následovně:
1) Na základě tabulky č. 2 je vybrán ten oxid, resp. hydroxid železa, kterým je voda nejvíce přesycena, tj. v daném případě hematit Fe2O3 a předpokládá se, že veškeré železo, které se uvolňuje do roztoku (0,059 mmol/l) se vysráží ve formě hematitu (0,029 mmol/l ~ 4,63 mg/l).
2) Při specifické hmotnosti hematitu 5,25 kg/l (Svoboda et al., 1960) se jedná o objemové množství 0,88 ml na jeden pórový objem reakční směsi, což odpovídá snížení pórovitosti o 0,00009 %.
Obdobným způsobem lze postupovat v případě kalcitu:
1) Kolonovou zkouškou bylo zjištěno snížení koncentrace vápníku ve vodě o cca 90 mg/l (tabulka č. 1). Předpokládejme, že veškerý vápník se vysrážel ve formě kalcitu (2,25 mmol/l ~ 225 mg/l).
2) Při specifické hmotnosti kalcitu 2,7 kg/l (Svoboda et al., 1960) se jedná o objemové množství 83,3 ml na jeden pórový objem reakční směsi, což odpovídá snížení pórovitosti o 0,0083 %.
Sečtením snížení pórovitosti vlivem vysrážení hematitu a kalcitu vychází celkové snížení o cca 0,0084 %. Z literatury vyplývá, že k nejintenzivnější korozi železných pilin dochází v prvních 15 cm reakční části stěny. Za předpokladu, že vysrážení minerálů nastává pouze po dobu průtoku vody touto zónou, lze na základě znalosti rychlosti proudění podzemních vod odhadnout snížení pórovitosti v čase.
Hydraulickým modelem proudění podzemních vod reakčními částmi plánovaných stěn na posuzované lokalitě byla odhadnuta průměrná rychlost proudění přibližně 0,17 m/den, což znamená dobu zdržení vody v úvodní části propustné stěny cca 1 den a tedy snížení pórovitosti o přibližně 3 % ročně.
Obdobným výpočtem bylo pro lokalitu NAS Moffett Field v USA odhadnuto roční snížení pórovitosti v rozmezí 4 - 11 % (Gavaskar et al. 2000). Po přibližně 1,5 ročním provozu reaktivní propustné stěny, pro kterou byl odhad proveden, nebyly však na lokalitě zaznamenány žádné významné hydraulické změny. Hlavním důvodem pravděpodobně je, že k vysrážení minerálů nedochází na povrchu železa, ale že sraženiny jsou ve formě koloidů unášeny proudem podzemní vody mimo reakční část stěny a předpokládané snížení pórovitosti nenastává.
Údaje získané z kolonové zkoušky a z výstupů modelu PHREEQC mohou být použity rovněž k odhadu rychlosti koroze reakční náplně.
Korozí železných pilin dochází k uvolnění 0,059 mmol/l železa, při odhadované pórovitosti 50 % a měrné hmotnosti použitých železných pilin 7,3 kg/l vychází rychlost koroze cca 0,45 mg/kg/den.
Závěr
Geochemické modelování je účinným prostředkem pro zjištění potenciálních procesů, které budou probíhat na propustných reaktivních stěnách pro sanaci rozpuštěných chlorovaných uhlovodíků. Nicméně jeho použití je závislé na množství vstupních dat. Jako nejvýhodnější se jeví použití modelu společně s výsledky z kolonových zkoušek. Bez těchto údajů může vést geochemické modelování vzhledem ke komplikovanosti procesů k chybným závěrům.
Dále je třeba zmínit, že i modelování podpořené výsledky experimentálních zkoušek je závislé na kvalitě databází použitých modelů, jako příklad lze uvést nezohlednění vysrážení hydroxidu železnatého, jehož precipitace je dle fázových diagramů FeII/FeIII (např. Pitter, 1999) za daných oxidačně-redukčních podmínek vysoce pravděpodobná. Pro zohlednění Fe(OH)2 však nejsou dostupná potřebná data o termodynamice (konstanta rozpustnosti, entalpie).
Údaje zjištěné geochemickým modelováním je možno následně použít k odhadům rychlosti koroze reakční náplně a snížení pórovitosti s ohledem na tvorbu sraženin. Z provedených odhadů vyplynulo potenciální snížení pórovitosti o přibližně 3 % ročně a to zejména vzhledem k vysrážení uhličitanu vápenatého (kalcitu).
Literatura
Ball J.W., D.K. Nordstrom a D.W. Zachmann, (1987): WATEQ4F – A Personal Computer FORTRAN Translation of the Geochemical Model WATEQ2 with Revised Database. U.S. Geological Survey Open File Report 87-50.
Gavaskar A. et al., (1997): Design Guidance for Application of Permeable Barriers to Remediate Dissolved Chlorinated Solvents. Air Force Research Laboratory, Battelle.
Gavaskar A. et al., (2000): Design Guidance for Application of Permeable Reactive Barriers for Groundwater Remediation. Air Force Research Laboratory, Battelle.
Kozubek P., (1995): Redox Processes And Other Geochemical Processes during Deep Artificial Recharge. TNO-report GC R-95-068(B), 46 p.
Parkhurst D.L., (1995): User's Guide to PHREEQC - A Computer Program for Speciation, Reaction-Path, Advective Transport, and Inverse Geochemical Calculations. U.S. Geological Survey, Water-Resources Investigations Report 95-4227, 143 p.
Pitter P., (1999): Hydrochemie. Vydavatelství VŠCHT Praha, 568 p.
Svoboda J.F. et al., (1960): Naučný geologický slovník. Nakladatelství ČSAV Praha.
Sweeny K.H., (1981): The Reductive Treatment of Industrial Wastewaters: I. Process Description. in Benett (ed.), American Institute of Chemical Engineers, Symposium Series, Water-1980, 77 (209): 67-71.